胸椎黄韧带骨化症术后脑脊液漏的相关因素
2023-09-05 我要说
来源:《中国矫形外科杂志》第31卷第9期
通信作者:周程沛 空军军医大学唐都医院
黄韧带骨化(ossification of ligamentum flavum,OLF)是引起胸椎管狭窄的最常见病因,其发病率较低,在中国人群中约占3.8%[1]。当出现胸脊髓症状,包括双下肢无力麻木、胸背部疼痛不适、胸腹束带感、间歇性跛行、二便功能障碍等,保守治疗效果不佳。手术是唯一有效治疗手段,以后路全椎板切除术为主要术式[2]。然术后脑脊液漏(cerebrospinal fluId leakage,CSFL)发生率较高,往往会导致切口愈合不良、感染、硬脊膜假性囊肿、神经根损伤等。
OLF人群发病率远低于腰椎疾病,临床上对CSFL的研究多集中于腰椎疾病,而对胸椎术后CSFL的研究较少,缺乏统一的认识。本研究回顾性分析后路全椎板切除减压术治疗的108例胸椎OLF患者的临床资料,为CSFL的预防和治疗提供依据。
1 资料与方法
1.1 纳入与排除标准
纳入标准:(1)诊断为胸椎黄韧带骨化症[3];(2)手术方式为后路全椎板切除术;(3)具有完整的病例资料及影像学数据(图1a~1e)。
排除标准:(1)联合其他部位的手术,如胸腰椎联合手术;(2)合并胸椎外伤、畸形、结核(3)既往有胸椎手术史。
1.2 一般资料
回顾性分析2015年8月—2021年8月患者的临床资料,共108例胸椎OLF患者符合上述标准,纳入本研究。男54例,女54例,平均年龄(54.7±11.6)岁。单节段OLF患者36例,双节段34例,多节段(≥3)38例。骨化物位于上胸椎8例,中胸椎8例,下胸椎92例。本研究获本院医学伦理委员会批准(第K202205-27号),所有患者均知情同意。
1.3 手术方法
全麻满意后,取俯卧位,常规消毒铺单。以责任节段为中心行后正中切口,逐步剥离椎旁肌肉,暴露棘突、椎板及关节突关节。“人”字嵴法定位椎弓根进针点,置入双侧椎弓根螺钉。咬骨钳咬除相应棘突,利用骨凿、高速磨钻或超声骨刀等器械沿双侧关节突中点纵行切口,传统组使用骨凿及椎板咬钳逐步揭除椎板,高速磨钻及超声骨刀组则采用整体揭盖式全椎板切除。
神经剥离子小心分离黄韧带与硬膜粘连部分,切除骨化黄韧带,探查上下节段椎管内空间,见无明显压迫,脊髓完全减压。打磨双侧关节突关节,适当植骨,后给予连接棒适当角度,安装内固定系统(图1f,1g)。
1.4 评价指标
一般资料:年龄、性别、BMI、病程时间、双下肢瘫痪、二便功能、基础病(高血压、糖尿病)、吸烟史、饮酒史、术前日本骨科协会改良评分(mJOA评分)。
影像学资料:OLF形态学分型,依据Sato分型分为外侧型、延伸型、肥厚型、结节型、融合型[4]。
椎管内侵占指标包括:椎管面积残余率,CT轴位椎管最狭窄处的横截面积与正常椎弓根平面椎管面积的比值;椎管正中前后径残余率,CT轴位最狭窄平面椎体后缘中点至骨化物的垂直距离与正常椎管正中线前后径的比值;椎管侧界前后径残余率,CT轴位侧界椎体后缘至骨化物的垂直距离与正常侧界前后径的比值;椎管旁正中线前后径残余率,正中线和侧界的中点垂直距离与正常旁正中线前后径的比值;矢状位椎管前后径残余率,CT矢状位测量椎体后缘至骨化物最突出的距离与正常椎管前后径的比值。正常椎管前后径及面积取邻近上下节段正常前后径和椎管面积之和的均值。对于多节段OLF患者,选取椎管面积残余率最低的节段进行分析。
手术资料:手术部位(上胸椎T1~4、中胸椎T5~8、下胸椎T9~12)、手术节段、手术工具、手术时间、失血量、住院时间。
CSFL诊断标准:(1)手术中硬膜破裂或有透明液体流出;(2)术后引流管持续排出大量淡红色血性液体,出现头疼、头晕、恶心等低颅压症状;(3)通过皮下穿刺或抽吸透明液体证实,或有影像资料确认(图1h)。
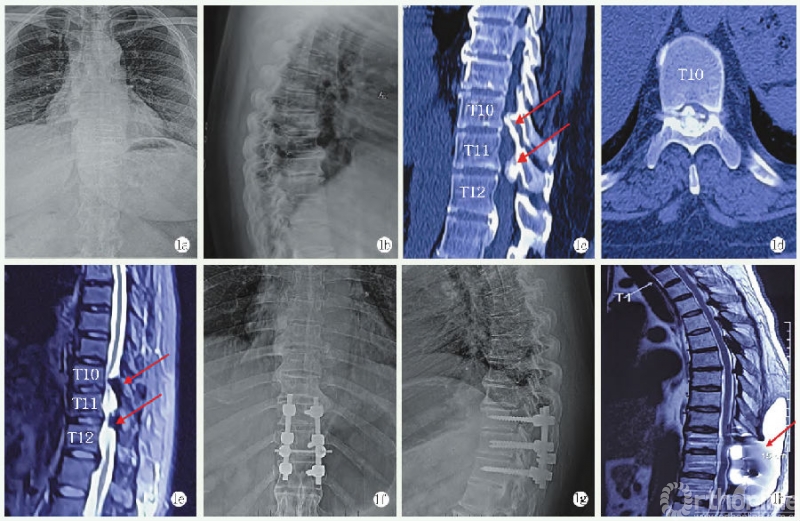
图1 患者女,48岁,胸椎黄韧带骨化症(T10/11、11/12)1a,1b:术前胸椎正侧位X线片;1c:矢状位CT示T10/11、T11/12黄韧带骨化;1d:轴位CT示T10/11严重椎管狭窄,Sato分型为结节型;1e:MRI示T10/11、T11/12黄韧带骨化,髓内高信号影;1f,1g:术后X线片见内固定位置良好;1h:术后MRI示CSFL并皮下积液
1.5 统计学方法
应用SPSS26.0软件对数据进行分析。计量数据以xˉ±s表示,资料呈正态分布时,两组间比较采用独立样本t检验,资料为非正态分布时,采用两样本秩和检验。计数资料采用x2检验或Fisher精确检验。以是否发生CSFL的二分类变量为因变量,其他因素为自变量行二元多因素逻辑回归分析。P<0.05为差异有统计学意义。
2 结果
2.1 临床结果
108例患者中28例并发CSFL,总体发生率25.9%。20例于术中发现有清亮液体自硬膜溢出,但破口较小未予特殊处理,仅严密缝合深筋膜层,术后5~7d据切口愈合情况拔除引流管。6例术后2~3d发现引流球中大量淡红色液体,考虑CSFL,给予延迟拔管并大量补液。2例于术后3d拔管,后发现皮下不明原因隆起,给予穿刺抽液。
2.2 是否发生CSFL的单项因素分析
以是否发生CSFL将患者分为两组,两组的各单项因素比较见表1。
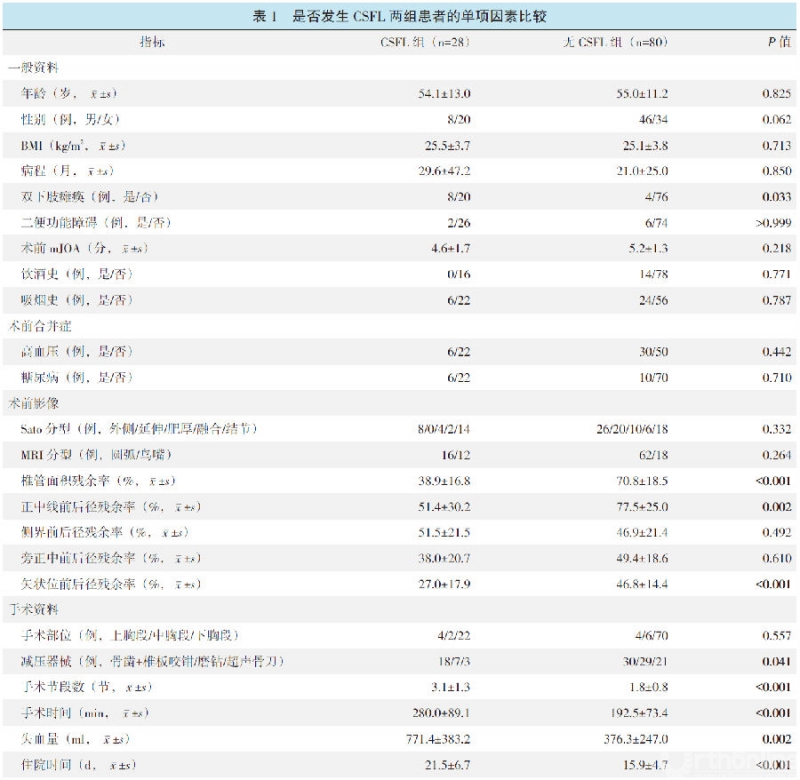
与无CSFL组相比,CSFL组术前双下肢瘫痪比率显著高(P<0.05);影像上椎管面积残余率、正中线前后径残余率、矢状位前后径残余率均显著小(P<0.05);此外,术中采用传统骨凿比率显著高(P<0.05),手术节段数显著多(P<0.05),手术时间和住院时间显著长(P<0.05)。两组年龄、性别、BMI、病程、二便功能障碍、术前mJOA、饮酒史、吸烟史、术前合并症(高血压、糖尿病)、Sato分型、MRI分型、侧界前后径残余率、旁正中前后径残余率及手术部位的差异无统计学意义(P>0.05)。
2.3 CSFL的二元多因素逻辑分析回归
以是否发生CSFL为因变量,手术节段数、手术时间数、椎管面积残余率、正中线前后径残余率、矢状位前后径残余率为自变量的多元逻辑回归分析就结果见表2。
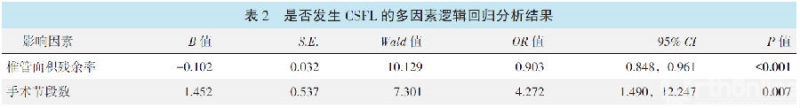
模型分类能力为74.1%,经卡方检验模型有效(x2=35.23,P<0.001)。结果表明,手术节段多(OR=4.272,P=0.007)、椎管面积残余率小(OR=0.903,P=0.001)是CSFL发生的独立危险因素。
3 讨论
不同脊柱节段术后CSFL的发生率大不相同。
Hannallah等[5]报道颈椎术后CSFL发生率仅1%。Tang等[6]报道腰椎术后CSFL发生率为3.6%。而胸椎术后CSFL发生率明显高于颈、腰椎手术。Wang等[7]报道胸椎术后CSFL发生率为12.1%。Hu等[8]报道胸椎术后CSFL发病率为32.3%。Xu等[9]对胸椎术后CSFL进行系统评价,发生率为22.5%。
本研究CSFL发生率为25.9%,与既往研究类似,发生率相对较高,可能由于双节段OLF患者34例,多节段(≥3)38例,占总病例的66.7%;其次,肥厚型、融合型及结节型占50%,其骨化物体积大,硬膜受压变薄甚至粘连;此外,早期手术并无超声骨刀等动力工具,更多依赖于椎板咬钳等工具[10]。
Li等[11]发现硬膜长期受压可致硬膜外脂肪减少,硬膜厚度变薄,减压时易导致CSFL。本研究中CSFL组病程时间长于无CSFL组,但差异无统计学意义。
钟军等[12]发现吸烟患者胸椎术后CSFL风险显著升高,认为硬脊膜结构及成分与筋膜组织相似,吸烟会使其厚度变薄。本研究中CSFL组和无CSFL组在吸烟方面无显著差异(P>0.05),可能与研究样本相对较少有关。此外钟军等认为中上胸椎管面积狭窄,术中操作空间受限,硬膜损伤概率大。本研究中上胸椎人数占比14.8%,未发现手术部位不同而引起CSFL发生差异。
Hu等[8]发现>52岁或手术节段≥3个是CSFL的高危因素。本研究中两组年龄结构相似,未发现显著差异;但每增加1个手术节段,CSFL风险增高3.3倍。原因可能在于较多的手术节段,硬膜骨化或粘连的风险增加,此外手术时间延长,术者疲劳程度增加,注意力下降等因素,均可能增加硬膜撕裂的风险。有研究指出使用超声骨刀相较于高速磨钻可显著降低硬脊膜撕裂发生率[13],本研究对比传统骨凿/椎板咬钳,发现随着高速磨钻及超声骨刀的应用,CSFL呈明显下降,然高速磨钻组与超声骨刀组CSFL发生率无显著性差异(P>0.05)。
由于黄韧带和硬膜之间的粘连(DA)和骨化(DO),OLF患者常发生硬膜撕裂。Ju等[14]发现CT“轨道征”及“逗号征”对于预测DA及DO具有高度意义。“轨道征”即高密度的OLF和DO之间有低密度的间隙,CT上似“双轨”;“逗号征”即OLF和DO形状在CT上似“逗号征”。
Prasad等[15]认为T2环征可预测D0,即T2序列脊髓周围有环状低信号边缘。此外,有研究指出当骨化物横截面积占位>55%时,应警惕DO存在[16]。Zhai等[17]认为脑脊液的横截面积代表脊髓代偿空间,当≤14.3%时,表示存在DO。
本研究发现,椎管面积残余率每减小10%,CSFL风险增高1.0倍。原因在于DA及DO发生概率增高。此外骨化物占位较大时,术中咬除难度增大,为了达到预期效果,术者尽量较多咬除骨化物,稍有不慎,便有可能损伤硬膜。骨化物形态也可能是CSFL的危险因素,本研究发现CSFL组肥厚型、融合型、结节型占比更高,达71.4%,但相较于无CSFL组差异无统计学意义,需扩大样本量进一步研究证明。
准确判断有无骨化物粘连,制定周密手术计划,术中小心分离尤为关键。
当发生硬膜损伤,仔细探查破损情况,若破口极小,使用明胶海绵压迫,术毕后留置引流管,严密缝合筋膜层及皮下层以确保切口良好愈合[18]。若破口>2.5cm时,使用6/0的无创线缝合[19],针距在2mm左右。若破口撕裂较大,可进行一期修复,修复材料包括脂肪、肌肉、筋膜移植物[20,21]、胶原蛋白基质[22]、纤维蛋白胶[23]、医用生物胶[24]、可吸收止血流体明胶[25]、人工硬脊膜补片等。术后常规去枕平卧位,密切观察引流液颜色及量,维持水电解质平衡。Sun等[21]则认为俯卧位可降低硬膜破口处的静水压,且脊髓向上漂浮封闭破口。对于切口愈合不佳者,可用腰大池置管引流术[26]。
本研究存在以下不足:(1)单中心研究,因OLF发病率低,病例数量较少,未来需进一步开展多中心、大样本量的研究;(2)回顾性研究,对于CSFL的判断多依赖于病例记录资料,需进一步进行前瞻性研究来确定研究结果;(3)由于样本量的限制,没有按手术节段进行亚组分析。
综上所述,后路全椎板切除减压术治疗OLF术后CSFL风险不容小视。对于多节段或椎管面积残余率较小者,术前应制定针对性的预防措施及处理办法,术中小心操作,利用显微镜、超声骨刀等工具,积极保护硬脊膜,避免术后CSFL的发生。
参考文献:





 京公网安备11010502051256号
京公网安备11010502051256号